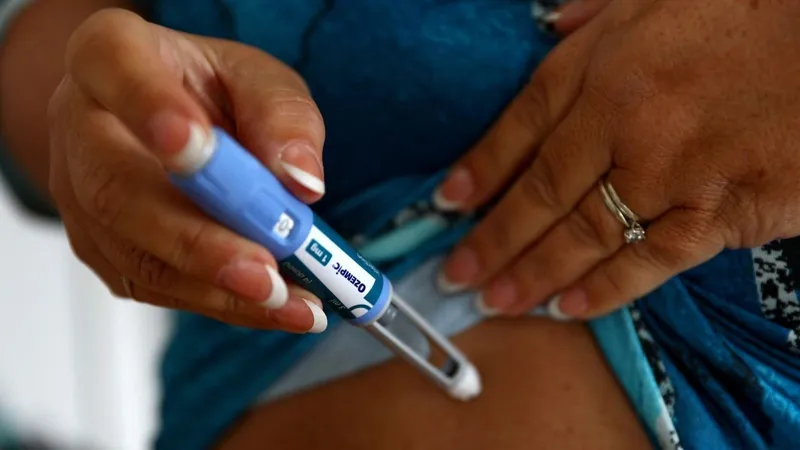
A Agência Nacional de Vigilância Sanitária anunciou nesta segunda-feira (6) um conjunto de medidas para combater irregularidades na importação e manipulação de medicamentos conhecidos como canetas emagrecedoras, utilizados no tratamento com agonistas de GLP-1.
As ações têm como objetivo ampliar a segurança de pacientes que utilizam substâncias como semaglutida, tirzepatida e liraglutida, diante do crescimento considerado irregular na produção e comercialização desses produtos no país.
Entre as principais iniciativas estão a revisão das regras atuais do setor, a intensificação da fiscalização em farmácias de manipulação e empresas importadoras, além da possibilidade de suspensão da autorização de funcionamento de estabelecimentos que apresentem risco sanitário.
Segundo a Anvisa, o aumento na manipulação desses medicamentos acendeu um alerta sobre a qualidade e a procedência dos insumos utilizados. Um levantamento da agência aponta que, apenas no segundo semestre de 2025, foram importados 130 quilos de insumos farmacêuticos — quantidade suficiente para a produção de cerca de 25 milhões de doses, número considerado incompatível com a demanda nacional.
Segundo a agência, apenas neste ano já foram realizadas 11 inspeções — número superior ao total de todo o ano de 2025 —, resultando na interdição de oito empresas, sendo sete farmácias de manipulação e uma importadora. As operações também levaram à apreensão de mais de 1,3 milhão de unidades de produtos estéreos.
De acordo com a Anvisa, trata-se da maior ofensiva já realizada no país contra irregularidades nesse tipo de medicamento.
Irregularidades e riscos sanitários
Durante a coletiva, dirigentes da agência detalharam uma série de problemas encontrados nas fiscalizações. Entre eles estão a comercialização de produtos sem registro sanitário, falhas graves de esterilidade — com risco de contaminação biológica —, uso de insumos sem origem comprovada e quebra da cadeia de refrigeração.
Também foram identificados casos de farmácias operando sem autorização de funcionamento, produção incompatível com a lógica da manipulação individualizada e ausência de prescrição médica vinculada aos produtos.
Outro ponto de preocupação é o uso indevido de marcas comerciais e a presença de estoques prontos para venda, prática que descaracteriza a manipulação magistral, que deve ser feita sob medida para cada paciente.
Mercado paralelo e falta de rastreabilidade
A Anvisa afirmou que há indícios de um mercado paralelo relevante envolvendo esses medicamentos, com entrada de produtos acabados sem registro e também de insumos farmacêuticos ativos (IFAs) de qualidade duvidosa.
Apesar disso, a agência reconhece que não há estimativas precisas sobre o tamanho desse mercado irregular, justamente pela ausência de controle e rastreabilidade.
“O que conseguimos identificar é a presença tanto de produtos falsificados quanto de manipulação inadequada e importações fora dos canais regularizados”, explicou a diretoria durante a coletiva.
A agência também confirmou que atua em conjunto com órgãos policiais e outras autoridades de fiscalização para combater esse tipo de prática.
Explosão na importação levanta alerta
O diagnóstico apresentado aponta ainda um crescimento expressivo na importação de insumos para esses medicamentos. Apenas entre novembro de 2025 e abril de 2026, mais de 100 quilos de tirzepatida foram importados por canais oficiais — volume suficiente para cerca de 20 milhões de doses.
Além disso, 14 pedidos de importação foram negados somente em março deste ano por problemas relacionados ao controle de qualidade.
Para a Anvisa, os números são incompatíveis com a demanda real e reforçam a suspeita de desvio para produção irregular ou comercialização fora das regras sanitárias.
Manipulação em larga escala sob suspeita
Embora a agência evite o termo “larga escala”, técnicos admitiram que há indícios de uso indevido do modelo de farmácia de manipulação para produção em volume, o que não é permitido pela regulamentação.
Pelas regras atuais, cada medicamento manipulado deve estar vinculado a uma prescrição individual, com identificação do paciente e do médico responsável. A produção prévia para estoque ou venda indiscriminada é considerada irregular e pode caracterizar atividade industrial sem autorização.
Novas regras e endurecimento do controle
Diante do cenário, a Anvisa anunciou um plano de ação com revisão de normas e endurecimento dos critérios de controle sanitário.
Entre as mudanças em discussão estão a exigência de certificação de boas práticas de fabricação para insumos importados, maior rastreabilidade ao longo da cadeia produtiva e regras mais rígidas para vinculação entre prescrição médica e produto manipulado.
A agência também avalia mudanças nos procedimentos de importação, incluindo a revisão de mecanismos atuais de liberação de insumos.
As propostas devem ser analisadas pela diretoria colegiada ainda em abril.
Aumento da oferta de produtos regulares
Paralelamente, a Anvisa informou que há 17 pedidos de registro de medicamentos com base em GLP-1 em análise, com prioridade na tramitação. A medida busca ampliar a oferta de produtos regularizados no mercado brasileiro.
A estratégia ocorre após o vencimento da patente da semaglutida no país, o que abriu espaço para novos fabricantes — desde que comprovem segurança, eficácia e qualidade.
Foco em segurança, não em restrição
Segundo a agência, o objetivo das medidas não é proibir a manipulação desses medicamentos, mas garantir que o processo ocorra dentro das normas sanitárias.
“A ação não é de restrição do mercado, mas de combate ao uso de produtos inadequados e de práticas que colocam em risco a saúde da população”, afirmou a diretoria.
A Anvisa também pretende ampliar ações de farmacovigilância, comunicação com a sociedade e cooperação internacional para enfrentar o problema.